2022年7月25日,成都海博为药业有限公司(简称“海博为药业”)自主研发的强透脑、抗耐药、可逆三代BTK抑制剂HBW-3-20已正式申报临床研究。该项目是继公司首个创新药HBW-3220胶囊获得临床默示许可之后的又一个临床研究项目申请,标志着海博为药业在小分子靶向创新药研究方面实现了新跨越。HBW-3-20是海博为药业开发的具有强透脑性的三代BTK(布鲁顿酪氨酸激酶)抑制剂,拟用于B细胞非霍奇金淋巴瘤,主要开发适应症为原发性/继发性中枢神经系统淋巴瘤(PCNSL/SCNSL)或可能累及中枢神经系统的弥漫大B细胞淋巴瘤(DLBCL)。

原发性中枢神经系统淋巴瘤(PCNSL)是一种起源于脑、软组织、脊髓或眼的原发性结外非霍奇金淋巴瘤亚型,90%以上的组织学病理类型为弥漫大B细胞淋巴瘤(DLBCL)。该病侵袭性强、进展快,与其他类型淋巴瘤相比,患者生存期短、预后差。流行病学研究显示,近年来,PCNSL的发病率呈上升趋势,约占所有脑部肿瘤的4%,占结外淋巴瘤的4%-6%,防治形势严峻,靶向药物的市场需求极为旺盛。布鲁顿酪氨酸激酶(BTK)是B细胞相关肿瘤的基本靶点,BTK抑制剂在淋巴瘤及白血病治疗方面已经取得了巨大成功,但是PCNSL/SCNSL发病部位独特,存在血脑屏障,大约95%以上的药物无法达到病变的脑部组织,大大增加了治疗难度。
HBW-3-20是海博为药业透脑创新药物开发平台开发的首个强透脑、抗耐药可逆的三代BTK抑制剂,与第一个被批准用于治疗复发或难治性PCNSL 的一代不可逆BTK抑制剂Tirabrutinib(日本小野制药开发)相比,在透脑性(大鼠透脑率:>60% VS ~10%)、有效性等关键成药性方面都有着突出的优势,且能克服Tirabrutinib第一代BTK抑制剂由于C481S突变产生的耐药性问题,开发价值巨大。
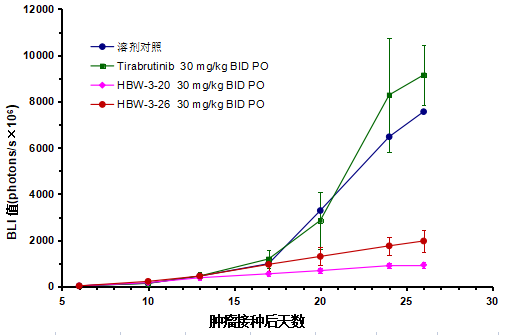

图片说明:临床前体内药效模型研究显示,HBW-3-20在30mg/kg BID剂量条件下,对脑部滤泡性淋巴瘤(DOHH2)具有明显的抑制作用,且明显优于Triabrutinib,并且耐受性较好
海博为药业坚持以临床需求为导向,以源头创新为驱动力,聚集了一支在药物研发全链条各环节有着深厚研发经验和强大执行力的管理团队,搭建了以开发能透过血脑屏障的药物为基础,形成以透脑药物分子设计、透脑药物分子合成及筛选、透脑药物药代动力学评价及毒理学研究为特色的专业、高效、系统化的透脑创新药物开发平台。除HBW-3-20已申报临床研究外,该平台其他创新药研发项目也在有序开展。我们真诚地向国内外药物研发同行发出邀请,希望能以开放式、多层次、多方位的合作模式,通过创新药区域权益转让、创新药和改良新药技术合作及技术转让等合作方式,成为志同道合的合作伙伴,开发出更多质优价更优的中国好药,践行良药济民的企业理念。
HBW-3220胶囊临床研究进展
2022年4月28日,HBW-3220胶囊在中国成熟B细胞淋巴瘤患者中的安全性、耐受性、有效性和药代动力学的多中心Ⅰ/Ⅱ期临床研究”正式启动,经过近三个月的临床试验,已顺利完成15mg、30mg两个剂量患者入组、给药的剂量爬坡研究。目前获得的PK数据显示HBW-3220胶囊具有良好的体内药代动力学行为、安全性好,并且在B细胞淋巴瘤的某些亚型中显示了初步的疗效趋势。预计将于2022年底完成I期剂量爬坡研究,进入剂量拓展和适应症拓展的IIa期临床研究阶段。

联系人:姜女士
电话:028-87014968
邮件:xiameijiang@hyperwaypharma.com
地址:成都市高新区科园南路88号天府生命科技园B4栋8楼